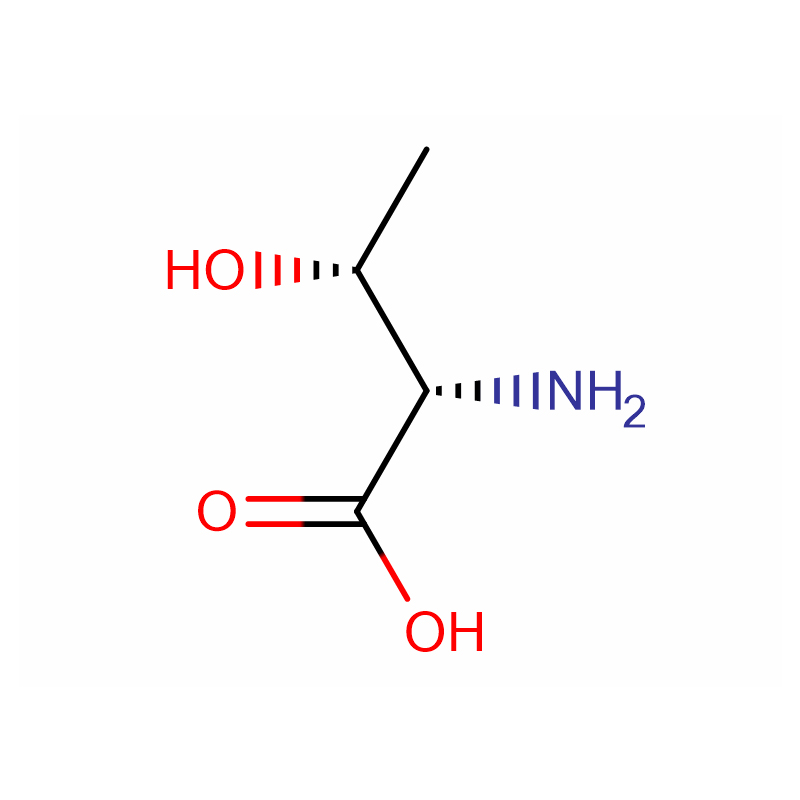
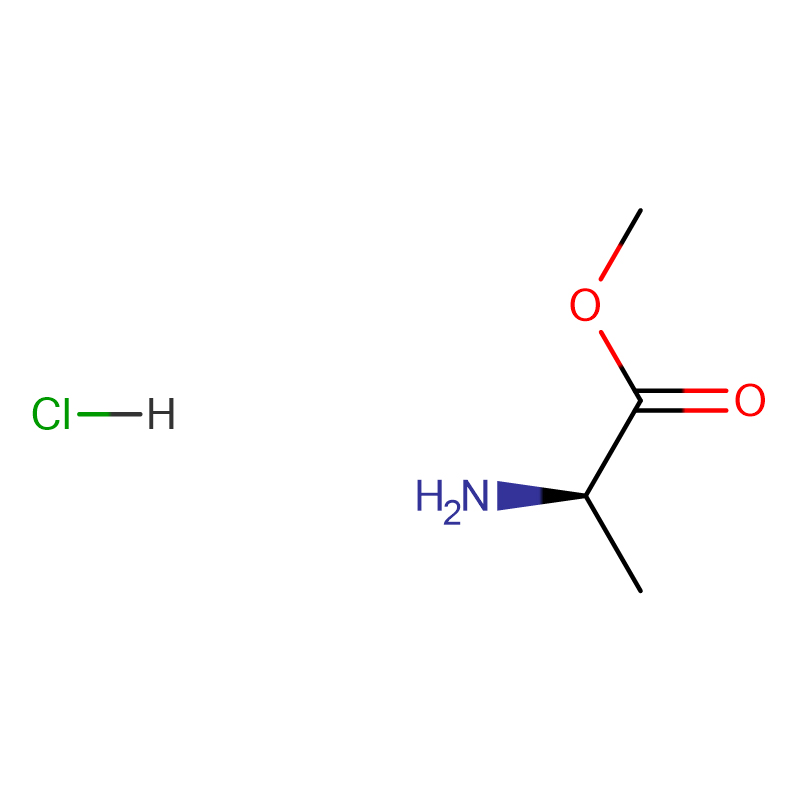
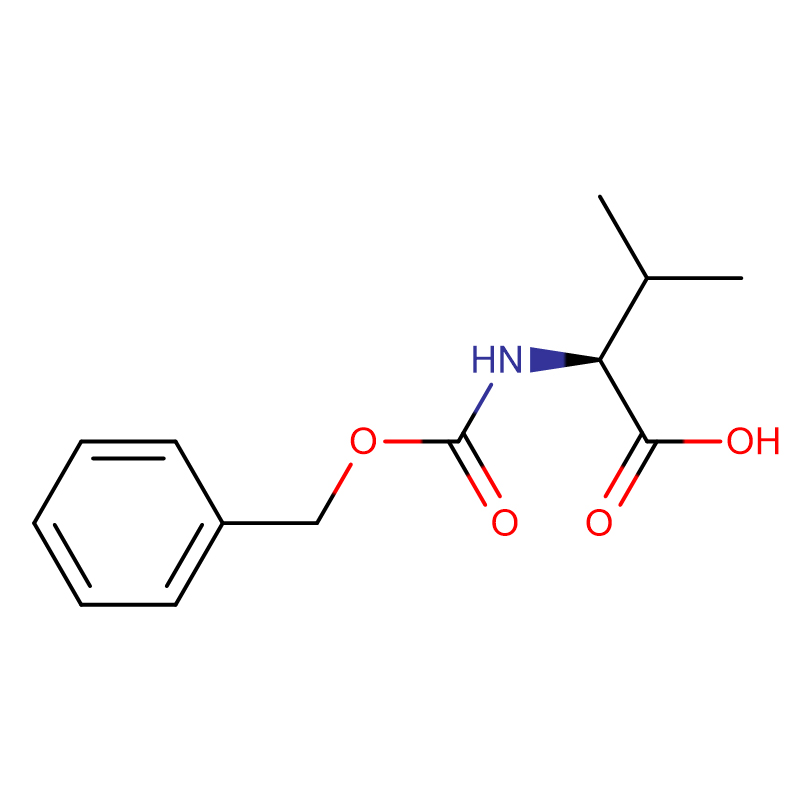
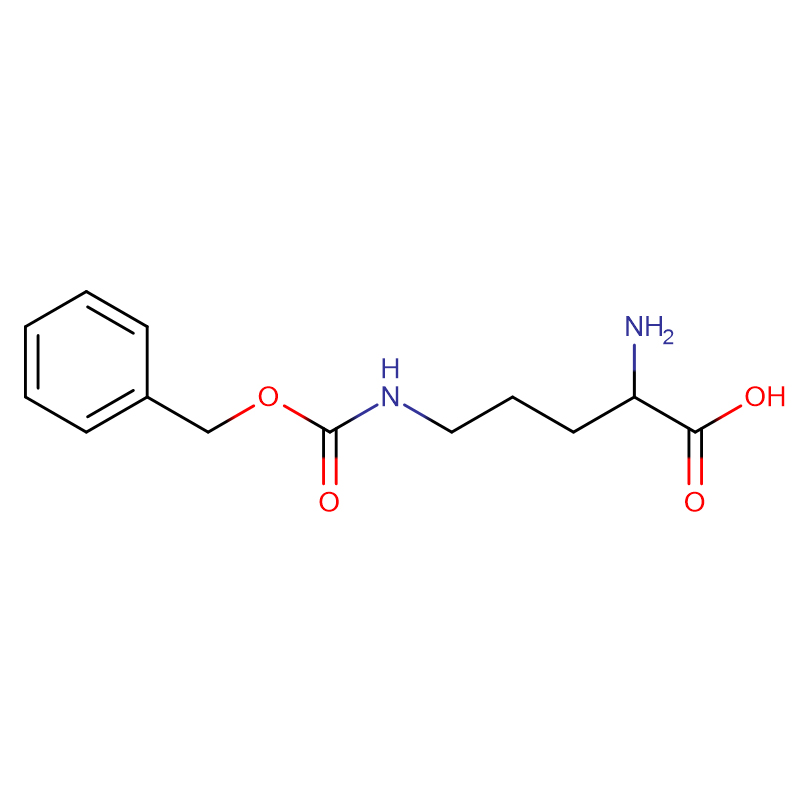
Kwas (2S,3R)-2-amino-3-hydroksybutanowy Cas: 72-19-5 99% Biały krystaliczny proszek
| Numer katalogu | XD90285 |
| Nazwa produktu | Kwas (2S,3R)-2-amino-3-hydroksybutanowy |
| CAS | 72-19-5 |
| Formuła molekularna | C4H9NO3 |
| Waga molekularna | 119.11916 |
| Szczegóły przechowywania | Otoczenia |
| Zharmonizowany kod taryfowy | 29225000 |
Specyfikacja produktu
| Analiza | 99 - 101% |
| Wygląd | Biały krystaliczny proszek |
| Dokładny obrót | -27,5 do -29,0 |
| Metale ciężkie | 10 str./min Maks. |
| AS | maks. 10 stron na minutę |
| pH | 5,2 - 6,5 |
| SO4 | <0,020% |
| Fe | maks. 10 stron na minutę |
| Strata przy suszeniu | <0,20% |
| Pozostałości po zapłonie | <0,10% |
| Przepuszczalność | NLT 98% |
| Cl | <0,02% |
| Sól amonowa | <0,02% |
Fosfatazy białkowe serynowo/treoninowe zostały opisane w wielu bakteriach chorobotwórczych jako niezbędne enzymy zaangażowane w szlaki przekazywania sygnału zależne od fosforylacji i często związane z wirulencją tych organizmów.Inspekcja genomu Mycoplasma synoviae wykazała obecność genu (prpC) kodującego domniemaną fosfatazę białkową z podrodziny fosfatazy białkowej 2C (PP2C).Tutaj przedstawiamy pełną charakterystykę biochemiczną fosfatazy M. synoviae (PrpC) i szczególną rolę jonów metali w relacji struktura-funkcja tego enzymu.Analiza sekwencji aminokwasowej PrpC ujawniła, że wszystkie reszty zaangażowane w dwujądrowe centrum metalu i domniemane reszty koordynujące trzeci jon metalu, konserwowane w fosfatazach PP2C, są obecne w PrpC.PrpC jest monomerycznym białkiem zdolnym do defosforylacji substratów fosfo z zależnością od jonów Mn(2+).Analiza stabilności termicznej wykazała stabilność enzymu w łagodnych temperaturach oraz wpływ jonów Mn(2+) na tę właściwość.Analiza spektrometrii mas sugeruje, że trzy jony metali wiążą się z PrpC, z których dwa mają pozorną stałą wysokiego powinowactwa.Analiza mutacji przypuszczalnych reszt koordynujących trzeci metal, Asp122 i Arg164, ujawniła, że te warianty wykazywały słabsze wiązanie jonów manganu i że obie mutacje wpłynęły na aktywność fosfatazy PrpC.Zgodnie z tymi wynikami, PrpC jest zależnym od metalu członkiem fosfatazy białkowej o ulepszonej stabilności w formie holo i Asp122, prawdopodobnie zaangażowanym w trzecie miejsce wiązania metalu, niezbędne dla aktywności katalitycznej.