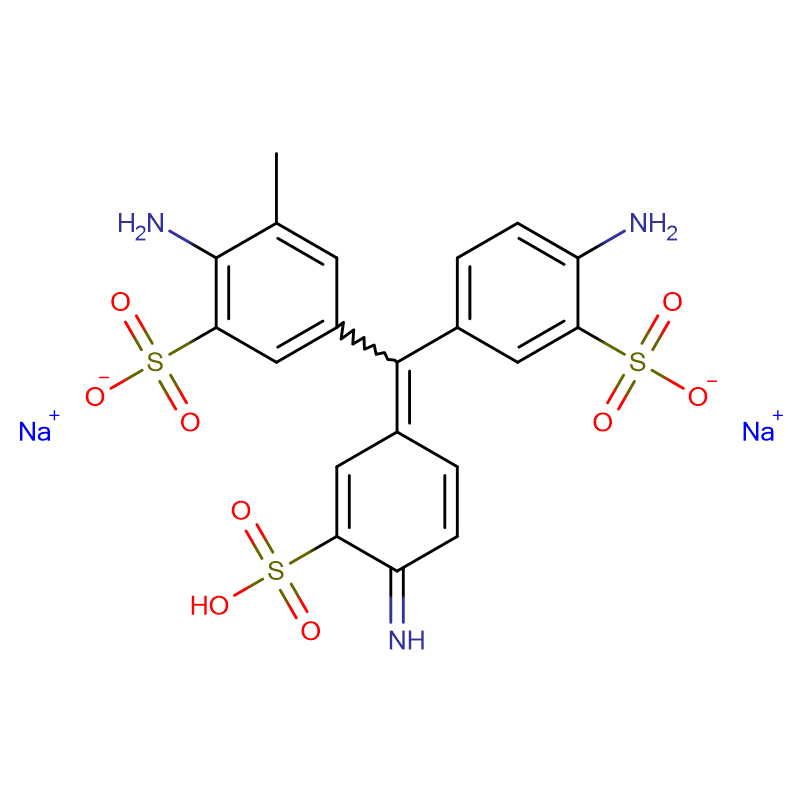
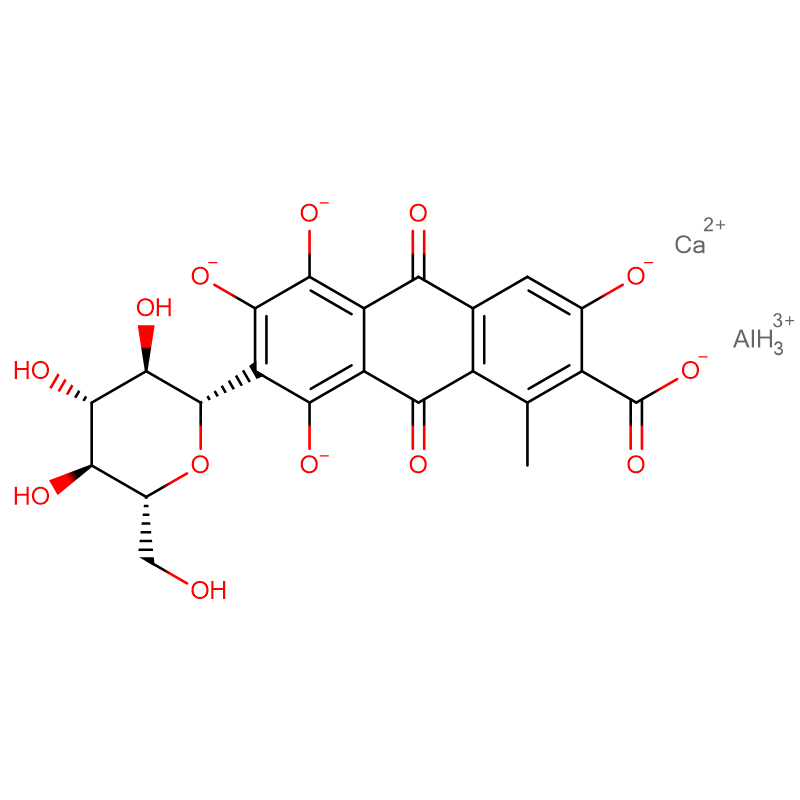
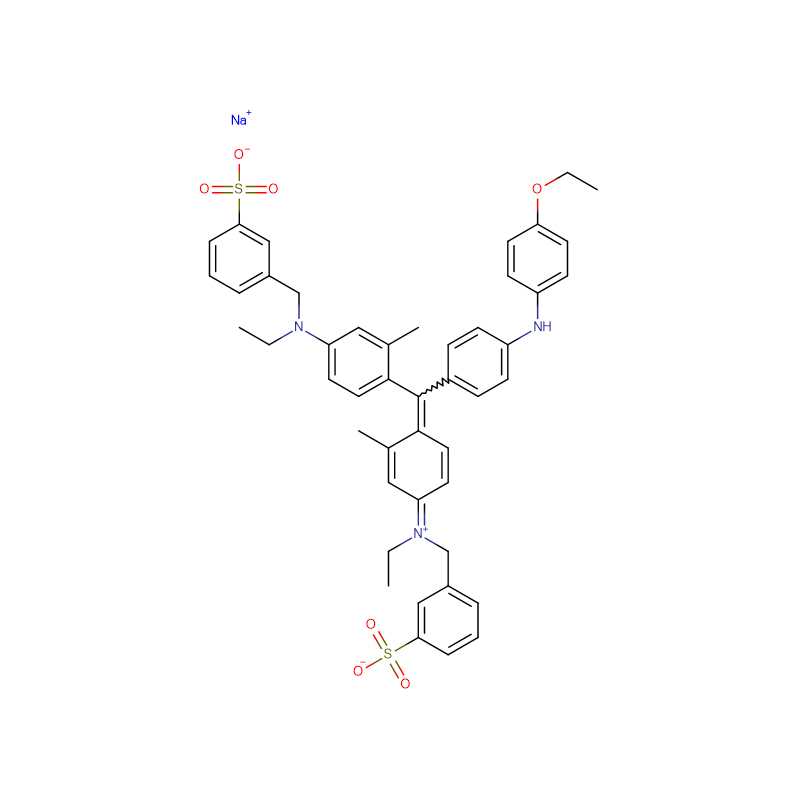
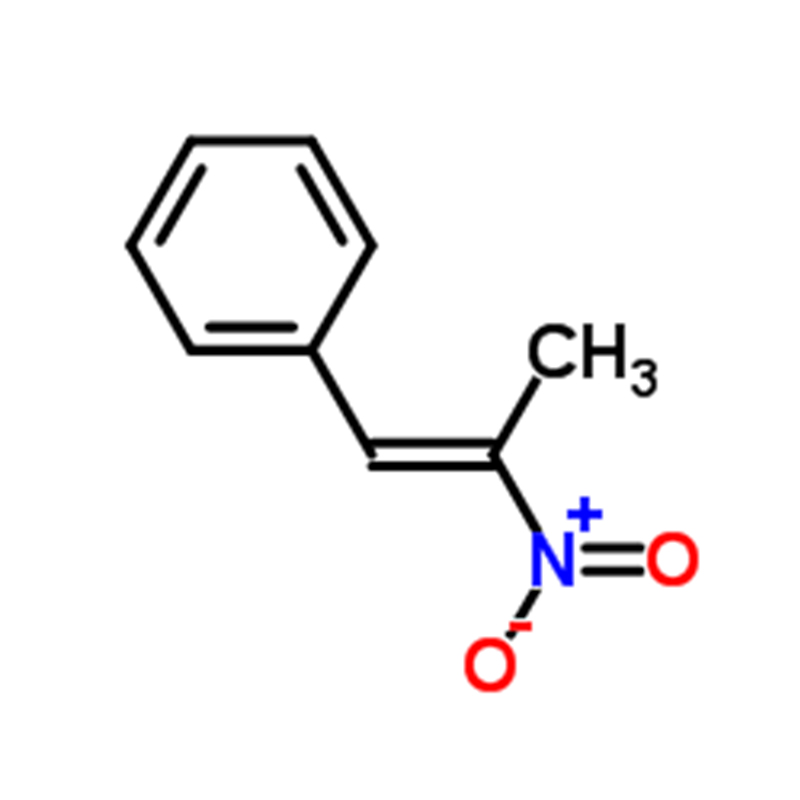
Kwas fuksynowy CAS:3244-88-0
| Numer katalogu | XD90488 |
| Nazwa produktu | Kwas fuksynowy |
| CAS | 3244-88-0 |
| Formuła molekularna | C20H20N2O9S3 |
| Waga molekularna | 585.5382 |
| Szczegóły przechowywania | Otoczenia |
| Zharmonizowany kod taryfowy | 32129000 |
Specyfikacja produktu
| Wygląd | ciemnozielony krystaliczny proszek |
| Analiza | 70% |
| Zawartość wody | 10,0% maks |
| Rozpuszczalność | Klarowny roztwór, bez cząstek |
| Wytrzymałość | 100% min |
| Nierozpuszczalne w wodzie | 0,2% maks |
Polipeptyd amyloidu wysepek (IAPP; znany również jako amylina) jest odpowiedzialny za tworzenie amyloidu wysepek w cukrzycy typu 2 i uważa się, że toksyczność indukowana przez IAPP przyczynia się do utraty masy komórek β związanej z późnymi stadiami cukrzycy typu 2.Tworzenie amyloidu wysepek może również odgrywać rolę w niepowodzeniu przeszczepu po przeszczepie.IAPP jest wytwarzany jako prohormon, pro-wysepkowy polipeptyd amyloidowy (proIAPP) i przetwarzany w ziarnistościach wydzielniczych komórek β trzustki.Częściowo przetworzone formy proIAPP znajdują się w złogach amyloidu;najbardziej godnym uwagi jest 48-resztowy związek pośredni, proIAPP(1-48), który zawiera N-końcowe pro-przedłużenie, ale które zostało odpowiednio przetworzone na C-końcu.Niekompletne przetwarzanie może odgrywać rolę w tworzeniu amyloidu wysepek poprzez promowanie interakcji z siarczanowanymi proteoglikanami macierzy zewnątrzkomórkowej, które z kolei promują tworzenie amyloidu.Pokazujemy, że kwaśna fuksyna (kwas 3-(1-(4-amino-3-metylo-5-sulfonianofenylo)-1-(4-amino-3-sulfonianofenylo)metyleno)cykloheksa-1,4-dienosulfonowy), prosty sulfonowana pochodna trifenylometylowa jest silnym inhibitorem tworzenia amyloidu przez produkt pośredni proIAPP(1-48).Bardziej skomplikowana pochodna trifenylometanu szybkozielona FCF {etylo-[4-[[4-[etylo-[(3-sulfofenylo)metylo]amino]fenylo]-(4-hydroksy-2-sulfofenylo)metylideno]-1-cykloheksa -2,5-dienylideno]-[(3-sulfofenylo)metylo]azan} również hamuje tworzenie amyloidu przez IAPP i produkt pośredni przetwarzania proIAPP.Oba związki hamują tworzenie amyloidu przez mieszaniny związku pośredniego proIAPP i modelowego siarczanu heparanu glikozoaminoglikanu.Kwaśna fuksyna hamuje również tworzenie amyloidu za pośrednictwem glikozoaminoglikanu przez dojrzały IAPP.Zdolność do hamowania tworzenia amyloidu nie wynika po prostu z sulfonowania związków, ponieważ sulfonowany inhibitor amyloidu-β, tramiprozat, nie jest inhibitorem tworzenia amyloidu przez proIAPP(1-48).