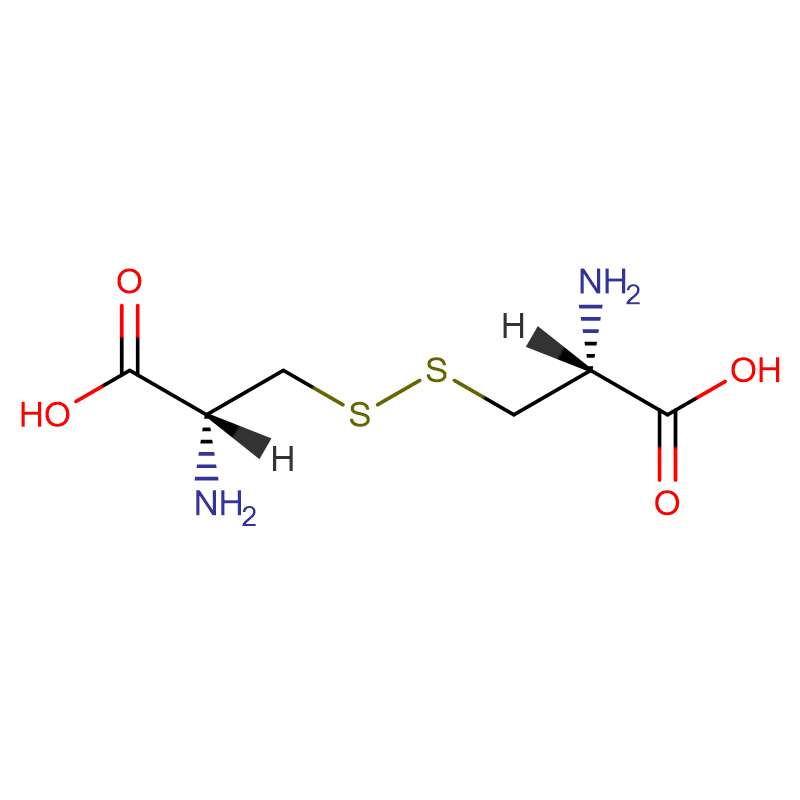
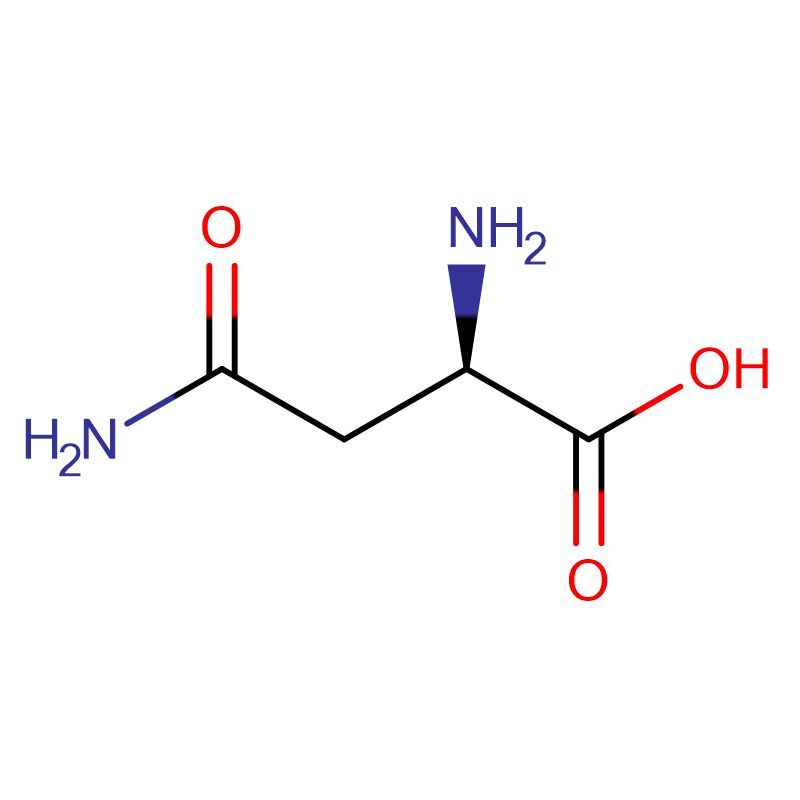
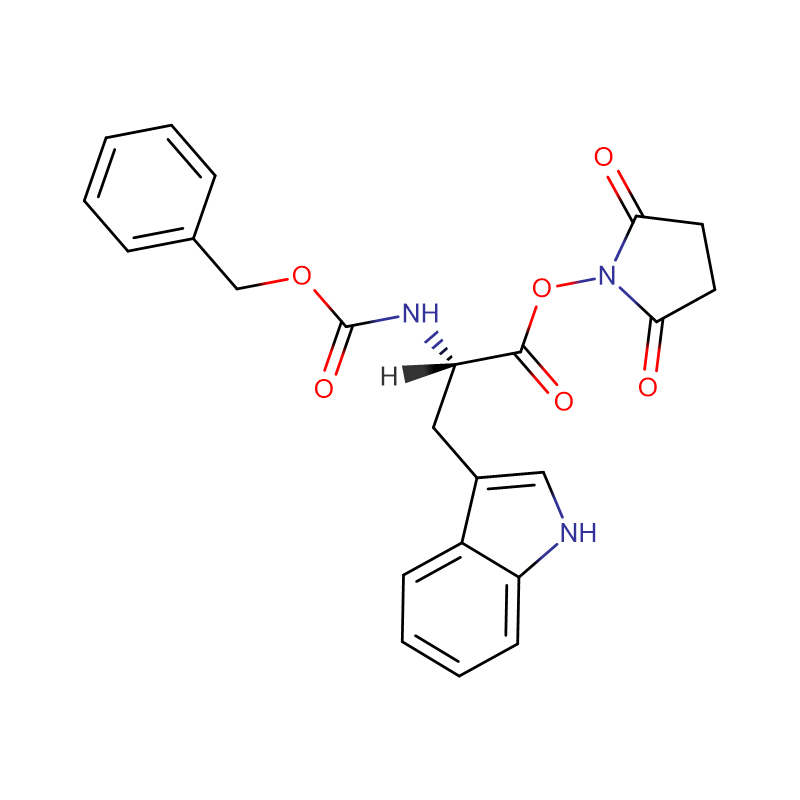
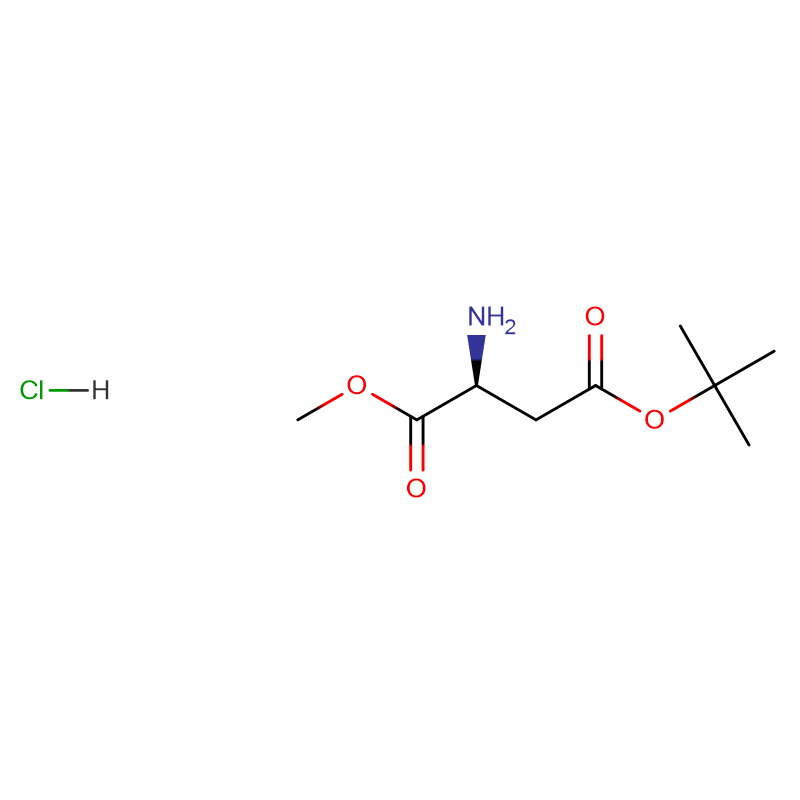
L-cystyna CAS:56-89-3 99% Białe kryształy lub krystaliczny proszek
| Numer katalogu | XD90322 |
| Nazwa produktu | L-cystyna |
| CAS | 56-89-3 |
| Formuła molekularna | C6H12N2O4S2 |
| Waga molekularna | 240,30 |
| Szczegóły przechowywania | Otoczenia |
| Zharmonizowany kod taryfowy | 29309013 |
Specyfikacja produktu
| Wygląd | Białe kryształy lub krystaliczny proszek |
| Analiza | 99% |
| Stopień | USP32 |
| Dokładny obrót | -215° do -225° |
| Metale ciężkie | <0,0015% |
| AS | maks. 1,5 ppm |
| SO4 | 0,040% maks |
| Fe | <0,003% |
| Strata przy suszeniu | 0,20% maks |
| Pozostałości po zapłonie | 0,10% maks |
| Cl | 0,10% maks |
Struktury krystaliczne kompleksów karboksypeptydazy T (CpT) z analogami substratów fenyloalaniny i argininy - kwasem benzylobursztynowym i kwasem (2-guanidynoetylomerkapto)bursztynowym - określono metodą wymiany molekularnej w rozdzielczościach 1,57 Å i 1,62 Å w celu wyjaśnienia szerokiego profilu specyficzności substratowej enzymu.Wykazano, że konserwatywne reszty Leu211 i Leu254 (również obecne zarówno w karboksypeptydazie A, jak i karboksypeptydazie B) są determinantami strukturalnymi do rozpoznawania substratów hydrofobowych, podczas gdy Asp263 był do rozpoznawania substratów naładowanych dodatnio.Mutacje tych determinant modyfikują profil substratowy: wariant CpT Leu211Gln uzyskuje właściwości podobne do karboksypeptydazy B, a wariant CpT Asp263Asn selektywność podobną do karboksypeptydazy A.Wykazano, że pętla Pro248-Asp258 oddziałująca z Leu254 i Tyr255 jest odpowiedzialna za rozpoznawanie C-końcowej reszty substratu.Wiązanie substratu w podmiejscu S1' prowadzi do zależnego od ligandu przesunięcia tej pętli, a ruch łańcucha bocznego Leu254 indukuje przegrupowanie konformacji reszty Glu277 kluczowej dla katalizy.Jest to nowy wgląd w selektywność substratową metalokarboksypeptydaz, który pokazuje znaczenie interakcji między podmiejscem S1' a centrum katalitycznym.