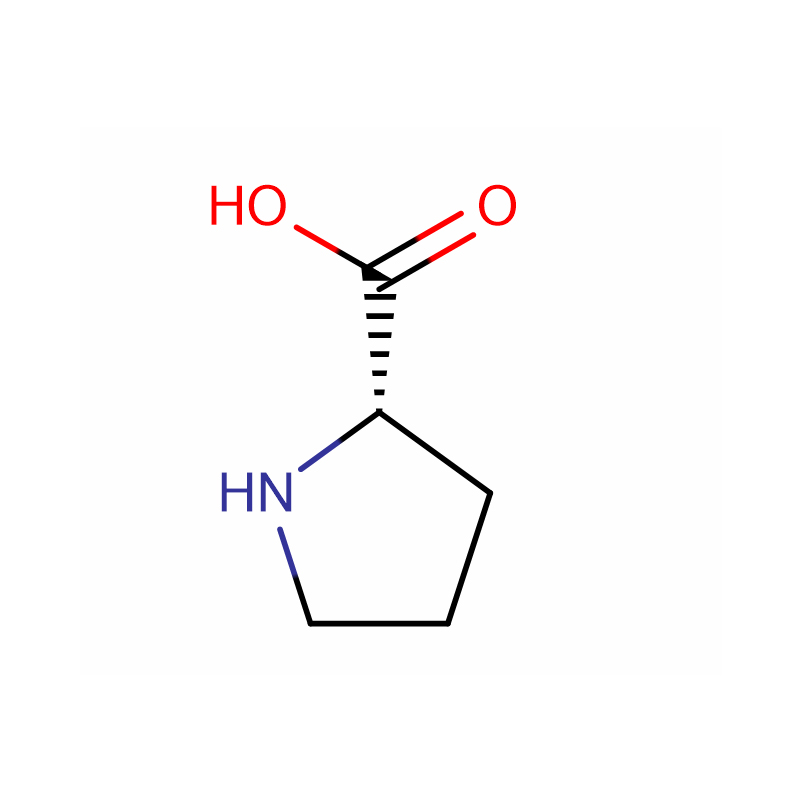
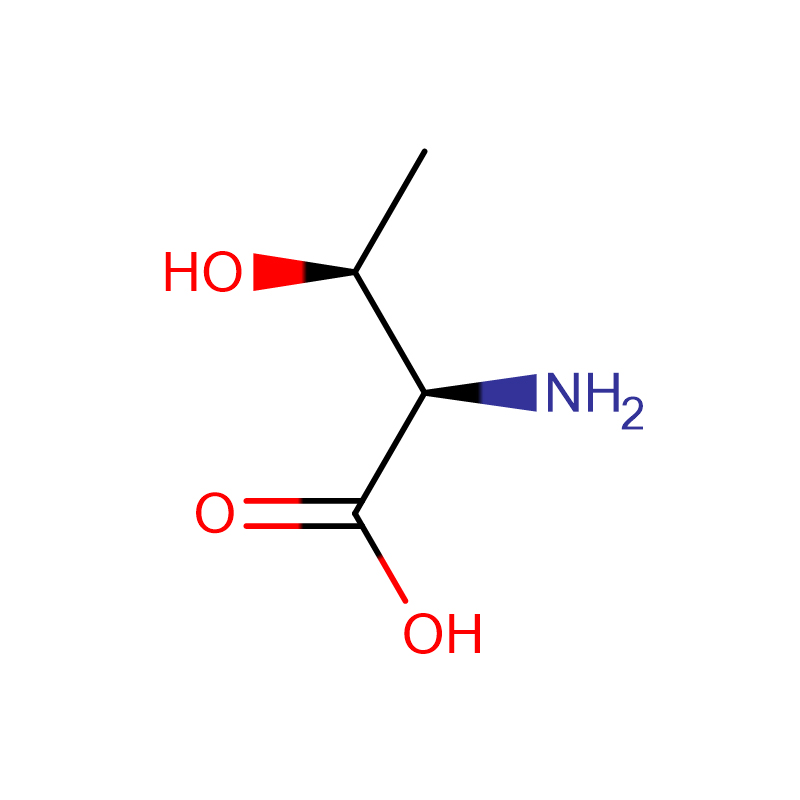
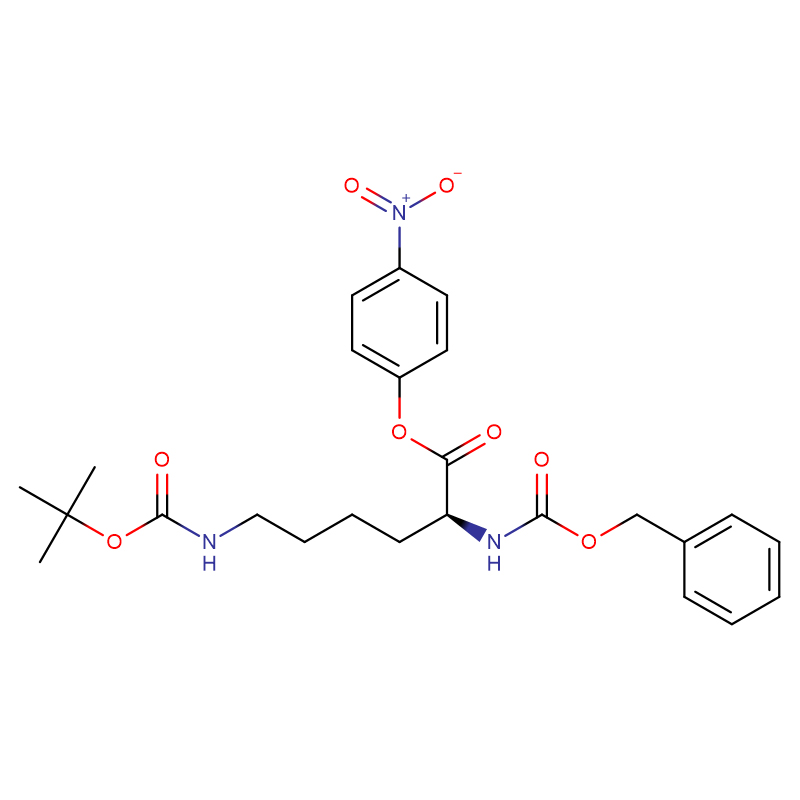
L-Proline Cas: 147-85-3 99% Biały proszek
| Numer katalogu | XD90293 |
| Nazwa produktu | L-Prolina |
| CAS | 147-85-3 |
| Formuła molekularna | C5H9NO2 |
| Waga molekularna | 115.13046 |
| Szczegóły przechowywania | Otoczenia |
| Zharmonizowany kod taryfowy | 29339980 |
Specyfikacja produktu
| Analiza | 99% min |
| Wygląd | biały proszek |
| Dokładny obrót | -84,5 do -86 |
| Metale ciężkie | <15 ppm |
| AS | <1ppm |
| Ph | 5,9 - 6,9 |
| SO4 | <0,050% |
| Fe | <30ppm |
| Strata przy suszeniu | <0,3% |
| Pozostałości po zapłonie | <0,10% |
| NH4 | <0,02% |
| Cl | <0,050% |
| Stan rozwiązania | >98% |
Zrozumienie metabolizmu mikrobiologicznego żywiciela jest niezbędne do rozwoju i optymalizacji procesów biokatalitycznych opartych na całych komórkach, ponieważ decyduje o wydajności produkcji.Jest to szczególnie prawdziwe w przypadku biokatalizy redoks, w której wykorzystuje się komórki aktywne metabolicznie ze względu na endogenną zdolność regeneracyjną kofaktora / kosubstratu w gospodarzu.Rekombinowana Escherichia coli została użyta do nadprodukcji 4-hydroksylazy proliny (P4H), dioksygenazy katalizującej hydroksylację wolnej L-proliny do trans-4-hydroksy-L-proliny z a-ketoglutaranem (a-KG) jako kosubstratem.W tym pełnokomórkowym biokatalizatorze centralny metabolizm węgla zapewnia wymagany kosubstrat a-KG, łącząc wydajność biokatalityczną P4H bezpośrednio z metabolizmem węgla i aktywnością metaboliczną.Stosując zarówno narzędzia biologii eksperymentalnej, jak i obliczeniowej, takie jak inżynieria metaboliczna i analiza przepływu (13)C-metabolicznego ((13)C-MFA), zbadaliśmy i ilościowo opisaliśmy fizjologiczną, metaboliczną i bioenergetyczną odpowiedź biokatalizatora pełnokomórkowego do ukierunkowanej biokonwersji i zidentyfikował możliwe wąskie gardła metaboliczne dla dalszej racjonalnej inżynierii szlaków. Skonstruowano szczep E. coli z niedoborem degradacji proliny przez usunięcie genu putA kodującego dehydrogenazę proliny.Biotransformacje całych komórek tym zmutowanym szczepem doprowadziły nie tylko do ilościowej hydroksylacji proliny, ale także do podwojenia specyficznej szybkości tworzenia trans-4-L-hydroksyproliny (hyp) w porównaniu z typem dzikim.Analiza przepływu węgla przez centralny metabolizm zmutowanego szczepu ujawniła, że zwiększone zapotrzebowanie a-KG na aktywność P4H nie zwiększyło strumienia generującego a-KG, co wskazuje na ściśle regulowaną operację cyklu TCA w badanych warunkach.W szczepie typu dzikiego synteza i kataliza P4H spowodowały zmniejszenie wydajności biomasy.Co ciekawe, szczep ΔputA dodatkowo kompensował związaną z tym utratę ATP i NADH, zmniejszając zapotrzebowanie na energię do utrzymania przy porównywalnie niskich szybkościach wychwytu glukozy, zamiast zwiększać aktywność TCA. Stwierdzono, że nokaut putA w rekombinowanej E. coli BL21 (DE3) (pLysS) być obiecujące dla produktywnej katalizy P4H nie tylko pod względem wydajności biotransformacji, ale także pod względem szybkości biotransformacji i wychwytu proliny oraz wydajności hip na źródle energii.Wyniki wskazują, że po nokaucie putA sprzężenie cyklu TCA z hydroksylacją proliny przez kosubstrat a-KG staje się kluczowym czynnikiem ograniczającym i celem dalszej poprawy wydajności biotransformacji zależnych od a-KG.