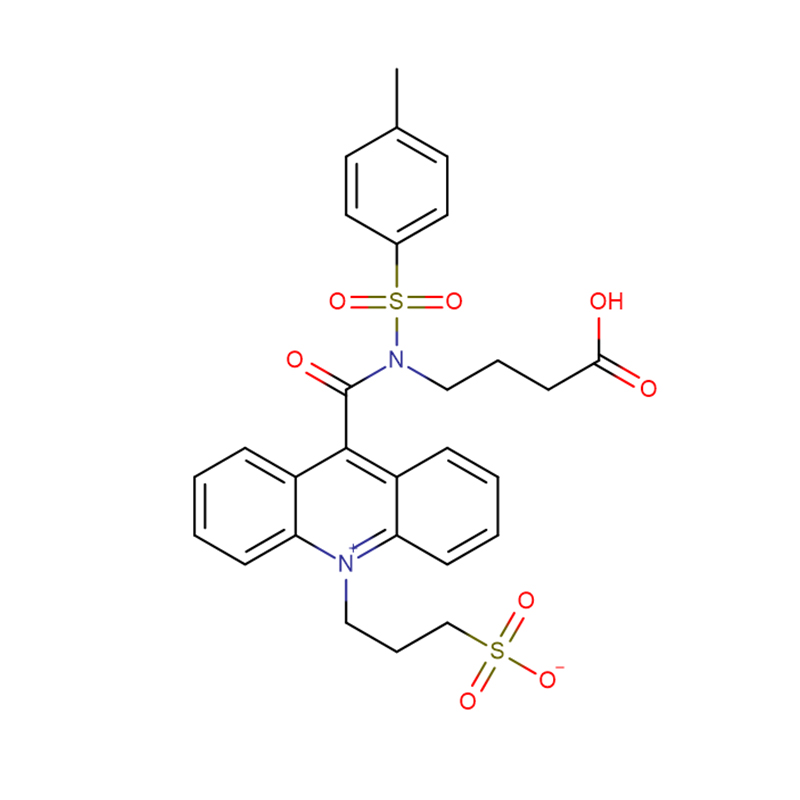
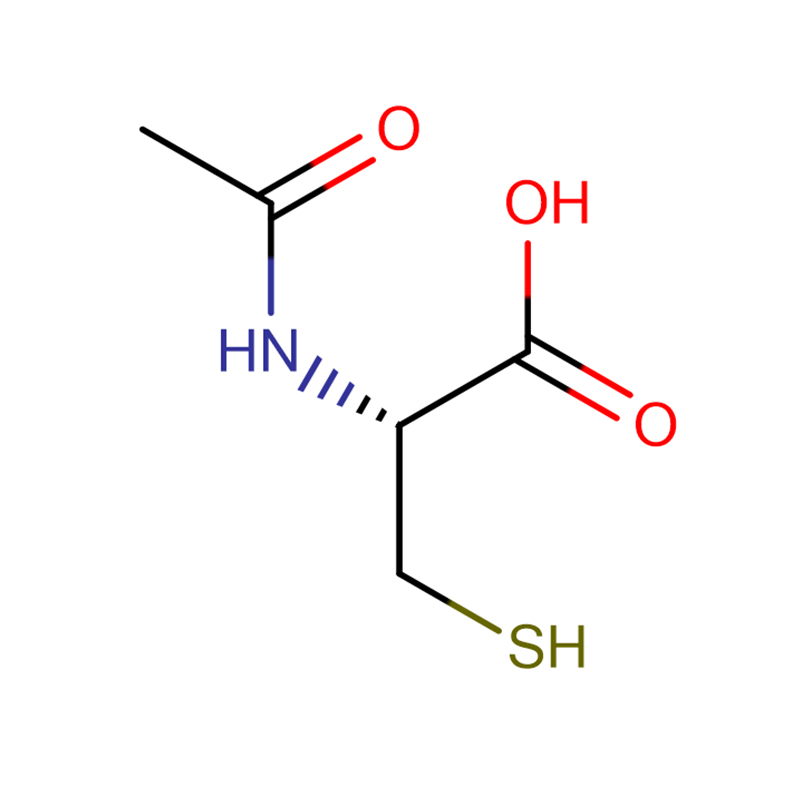
4-Amino-3-hydrazyno-1,2,4-triazol-5-tiol Cas:28836-03-5 99% Żółte do zielonego ciało stałe
| Numer katalogu | XD90146 |
| Nazwa produktu | 4-amino-3-hydrazyno-1,2,4-triazol-5-tiol |
| CAS | 28836-03-5 |
| Formuła molekularna | C16H13NO3S·NH3 |
| Waga molekularna | 316,37 |
| Szczegóły przechowywania | Otoczenia |
| Zharmonizowany kod taryfowy | 2923900090 |
Specyfikacja produktu
| Wygląd | Żółta do zielonej substancji stałej |
| Asay | ≥ 99% |
| Temperatura topnienia | 237°C(rozkład)(świeci) |
| Rozpuszczalność | NaOH: rozpuszczalny1 N |
| Rozpuszczalne w wodzie | Rozpuszczalny w wodzie, 1N NaOH i metanolu. |
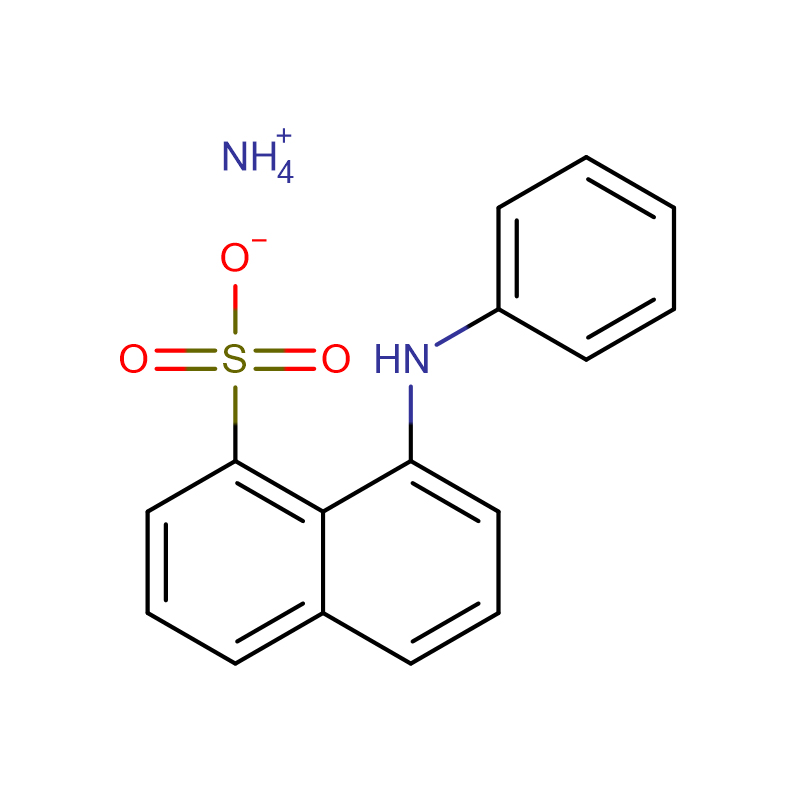
1. Zbadaliśmy hamujący wpływ izorhamnetyny na tyrozynazę grzybową za pomocą kinetyki hamowania i symulacji obliczeniowej.Izorhamnetyna odwracalnie hamowała tyrozynazę w sposób mieszany przy Ki=0,235±0,013 mM.Pomiary fluorescencji wewnętrznej i wiązania 1-anilinonaftaleno-8-sulfonianu (ANS) wykazały, że izorhamnetyna nie indukowała istotnych zmian w strukturze trzeciorzędowej tyrozynazy.Aby uzyskać wgląd w proces inaktywacji, kinetykę obliczono za pomocą pomiarów przedziałów czasowych i ciągłych reakcji substratów.Wyniki wskazują, że inaktywacja indukowana przez izorhamnetynę była reakcją pierwszego rzędu z procesami dwufazowymi.Aby uzyskać więcej informacji, symulowaliśmy dokowanie między tyrozynazą a izorhamnetyną.Symulacja przebiegła pomyślnie (energia wiązania dla Dock6.3: -32,58 kcal/mol, dla AutoDock4.2: -5,66 kcal/mol i dla Fred2.2: -48,86 kcal/mol), co sugeruje, że izorhamnetyna oddziałuje z kilkoma pozostałościami, takimi jak jako HIS244 i MET280.Ta strategia przewidywania interakcji tyrozynazy w połączeniu z kinetyką opartą na związku flawanonowym może okazać się przydatna w badaniach przesiewowych pod kątem potencjalnych naturalnych inhibitorów tyrozynazy.
2. Ścieżka rozwoju kwasowego konalbuminy (CA), monomerycznej glikoproteiny z białka jaja kurzego, została zbadana przy użyciu spektroskopii CD dalekiego i bliskiego UV, wewnętrznej emisji fluorescencji, zewnętrznej sondy fluorescencyjnej sulfonianu 1-anilino-8-naftalenu (ANS) i dynamiczne rozpraszanie światła (DLS).Obserwujemy zależne od pH zmiany drugorzędowej i trzeciorzędowej struktury CA.Ma natywną α-helikalną strukturę drugorzędową przy pH 4,0, ale strukturę stratną przy pH 3,0.CA istniał wyłącznie w postaci wstępnie stopionych kuleczek i stopionych kuleczek w roztworze odpowiednio przy pH 4,0 i pH 3,0.Wpływ pH na konformację i termostabilność CA wskazuje na jego odporność na ciepło przy obojętnym pH.Wyniki DLS pokazują, że stan MG istniał w postaci zwartej w roztworach wodnych o promieniu hydrodynamicznym 4,7 nm.Wygaszenie fluorescencji tryptofanu przez akryloamid dodatkowo potwierdziło akumulację stanu pośredniego, częściowo niesfałdowanego, pomiędzy stanami natywnymi i niesfałdowanymi.




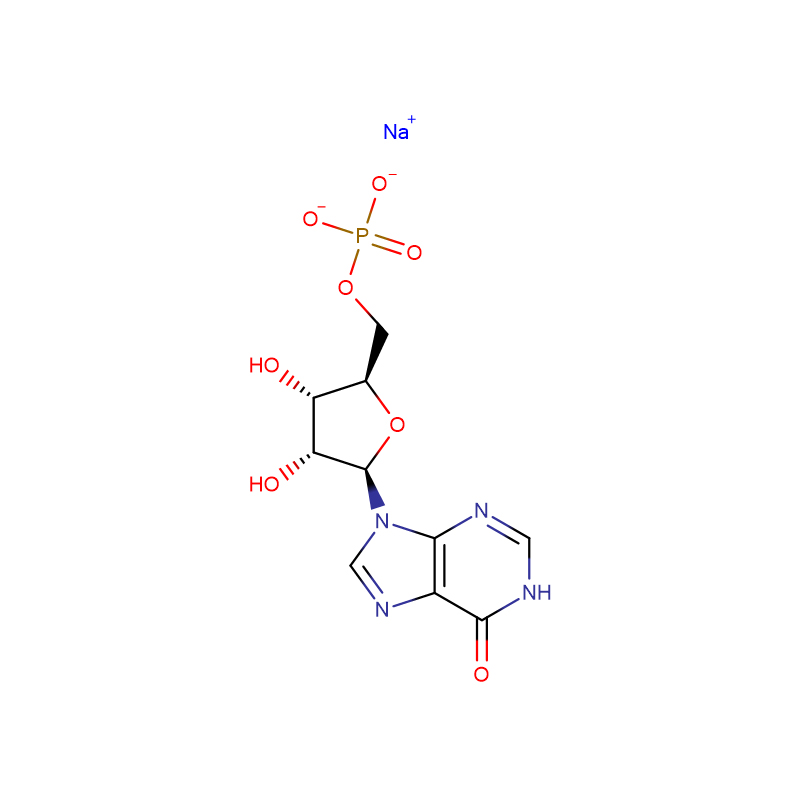
![Sól sodowa N-[[bis[4-(dimetyloamino)fenylo]amino]karbonylo]glicyny Biały do szarozielonego krystaliczny proszek](http://cdn.globalso.com/xdbiochems/115871-19-7.jpg)