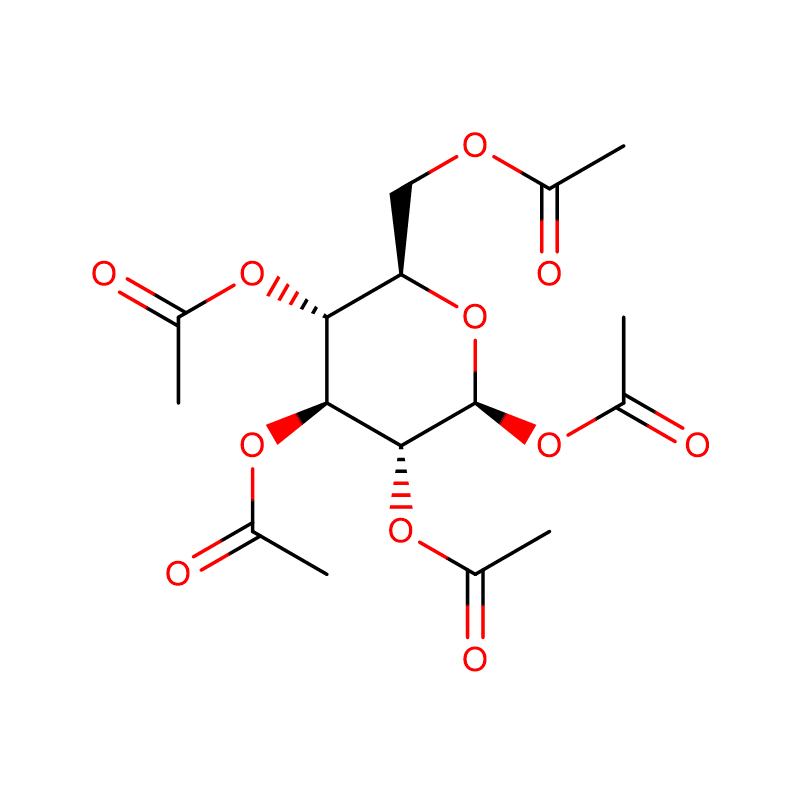
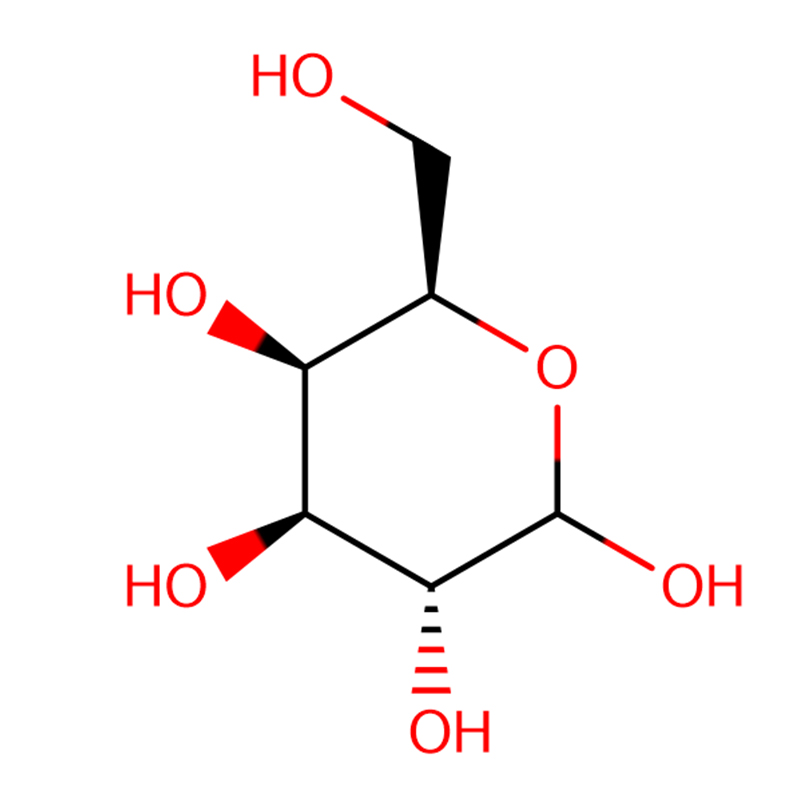
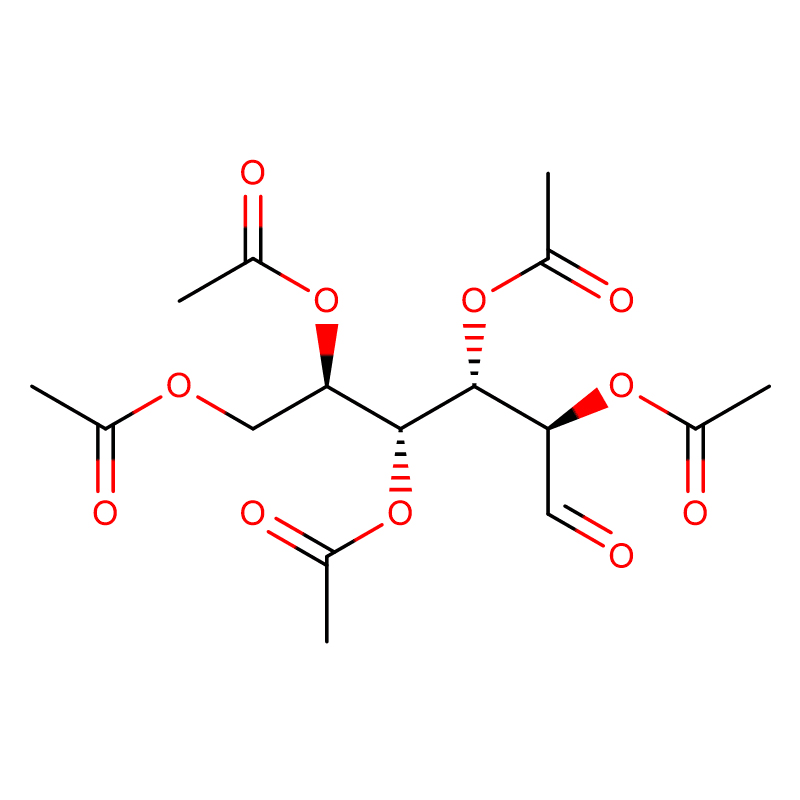
4-NITROPHENYL-ALPHA-D-MANNOPYRANOSIDE CAS: 10357-27-4 białawy proszek 98%
| Numer katalogu | XD90011 |
| Nazwa produktu | 4-nitrofenylo-alfa-D-mannopiranozyd |
| CAS | 10357-27-4 |
| Formuła molekularna | C12H15NO8 |
| Waga molekularna | 30301,25 |
| Szczegóły przechowywania | -2Do -8°C |
| Zharmonizowany kod taryfowy | 29400000 |
Specyfikacja produktu
| Woda | <5% Karla Fischego |
| Rozpuszczalność | 1% w DMF jest klarowny i bezbarwny |
| Czystość | Wolny 4-nitrofenol <200ppm |
| HPLC | >98% |
| Wygląd | Białawy proszek |
Mechanistyczny wgląd w zależną od Ca2 + rodzinę alfa-mannozydaz w ludzkim symbioncie jelitowym.
Bakterie okrężnicy, których przykładem jest Bacteroides thetaiotaomicron, odgrywają kluczową rolę w utrzymaniu zdrowia ludzkiego poprzez wykorzystywanie dużych rodzin hydrolaz glikozydowych (GH) do wykorzystywania polisacharydów dietetycznych i glikanów gospodarza jako składników odżywczych.Przykładem takiej ekspansji rodziny GH są 23 glikozydazy z rodziny GH92 kodowane przez genom B. thetaiotaomicron.Tutaj pokazujemy, że są to alfa-mannozydazy, które działają poprzez pojedynczy mechanizm przemieszczania w celu wykorzystania N-glikanów gospodarza.Trójwymiarowa struktura dwóch mannozydaz GH92 definiuje rodzinę dwudomenowych białek, w których centrum katalityczne znajduje się na granicy między domenami, zapewniając kwas (glutaminian) i zasadę (asparaginian) pomoc w hydrolizie w Ca(2+)- sposób zależny.Trójwymiarowe struktury GH92 w kompleksie z inhibitorami zapewniają wgląd w specyficzność, mechanizm i szlak konformacyjny katalizy.Ca(2+) odgrywa kluczową rolę katalityczną w pomaganiu w odkształcaniu mannozydu od konformacji krzesła w stanie podstawowym (4)C(1) w kierunku stanu przejściowego.(Bibliografia: Nat.chemiaBiol.6, 125-32, (2010)
Chromatografia powinowactwa czołowego glikoasparagin albuminy jaja kurzego na kolumnie A-Sepharose z konkanawaliną.Ilościowe badanie specyficzności wiązania lektyny.
Interakcje konkanawaliny A (ConA) unieruchomionej na Sepharose 4B z 10 glikoasparaginami pochodzącymi z albuminy jaja kurzego badano ilościowo metodą chromatografii powinowactwa czołowego.W tej metodzie roztwór węglowodanów jest nanoszony w sposób ciągły na kolumnę ConA-Sepharose i opóźnienie czoła elucji jest mierzone jako parametr siły oddziaływania.Można wyznaczyć stałą dysocjacji (Kd) dla każdego sacharydu z ConA.Analiza wiązania p-nitrofenylo-alfa,D-mannozydu wykazała, że właściwości wiązania ConA nie zmieniają się zasadniczo po unieruchomieniu na Sepharose 4B.Do analizy każdą z glikoasparagin albuminy jaja kurzego znakowano trytem metodą redukcyjnej metylacji.Porównanie otrzymanych wartości Kd wykazało, że wiązanie ConA różni się znacznie przy bardzo niewielkich różnicach strukturalnych łańcucha glikozylowego.Wyniki sugerują, że ConA rozpoznaje specyficzną strukturę łańcucha glikozylowego, Man alfa 1-6 (Man alfa 1-3) Man, w której co najmniej jedna grupa hydroksylowa w pozycji C-3 mannozy połączonej C-6 powinna być wolna.